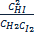Метод Мора



Метод Мора является одним из аргентометрических методов. Все эти методы основаны на реакции:
Аg + + Наl — → АgНаl↓
Метод Мора является наиболее простым из всех методов аргентометрии и в то же время достаточно точным. Титрантом является раствор нитрата серебра АgNОз 0.1 моль/л.
В основу метода Мора положена реакция взаимодействия ионов серебра с С1 — или Вг — .
Индикатором является хромат калия К2СгО4 5 %. Установочным веществом для определения титра раствора является NаС1 или КС1 0.1 моль/л.
Метод Мора позволяет определить количество хлоридов или бромидов. Иодиды этим методом не определяют, так как выпадающий в осадок иодид серебра АgI сильно адсорбирует К2СгО4, поэтому точку эквивалентности определить невозможно.
Растворимость АgСl значительно меньше, чем растворимость Аg2СгO4. Поэтому если постепенно добавлять раствор АgNOз к раствору, содержащему Сl — и CrO4 2- , то ПРAgС| достигается раньше ПР Аg2СгO4.
Это означает, что вначале образуется труднорастворимая соль
После того как хлорид-ионы будут практически полностью выделены в виде АgС1, появляется осадок. Происходит изменение окраски титруемой смеси и таким образом определяется конец титрования.
При титровании раствора бромида происходит аналогичное явление. Так как ПРАgВг + + 2OH — → Ag2O↓ + H2O
2. Определение нельзя проводить в присутствии ионов Ва 2+ , Вi 3+ , Рb 2+ , так как эти ионы образуют с ионами СгО4 2 — осадки.
3. Титрование всегда ведут от галогенида к АgNOз (т. е. галогенид титруют раствором АgNОз, а не наоборот). Только при таком условии кирпично-красный осадок Аg2СгО4 образуется в точке эквивалентности.
Метод Мора находит широкое применение при анализе пищевых продуктов. Количество поваренной соли в колбасе, соленой рыбе, масле и других продуктах определяют по методу Мора.
Этот метод применяется также для определения хлоридов в воде. Метод Мора используется и при анализе некоторых фармацевтических препаратов, например хлоридов и бромидов натрия и калия.
Определение хлоридов методом Мора
Приготовление титранта 0.05 моль/л раствора. Нитрат серебра не относится к тем веществам, из которых можно приготовить раствор заданной концентрации по точно взятой навеске. Поэтому готовят раствор примерно требуемой концентрации, а его титр устанавливают. Необходимую навеску (8.5 г AgNОз на 1 л раствора) отвешивают с точностью до 0.1 г на технических весах, и нужное количество воды отмеривают мерным цилиндром. Раствор сохраняют в темноте, так как на свету нитрат серебра разлагается. Однако и при надлежащем хранении титр раствора АgNОз меняется с течением времени и его необходимо время от времени проверять.
Приготовление установочного раствора. Для приготовления 0.05 моль/л, раствора NаС1 отвешивают на аналитических весах 0.2922 г NаС1 и количественно переносят в мерную колбу вместимостью 100 мл. Растворяют навеску в дистиллированной воде, доводят раствор до метки и хорошо перемешивают. Таким образом получают раствор NаС1.
Определение титра нитрата серебра. В качестве индикатора применяют 5 % раствор хромата калия К2СгО4 в воде. Наполняют бюретку раствором нитрата серебра АgNОз. Отобрав пипеткой 10 мл 0.05 моль/л раствора NаС1, переносят ее в колбу Эрленмейера вместимостью 250 мл, добавляют 0.5 мл раствора индикатора, немного разбавляют водой и медленно титруют 0.1 моль/л раствором АgNОз, непрерывно перемешивая жидкость до появления первого неисчезающего изменения цвета суспензии. Нужно уловить момент, когда лимонно-желтый цвет суспензии приобретет от капли АgNОз слегка красноватый оттенок. Запись анализа и расчеты производят так же, как при определениях кислотно-основным методом.

Определение хлорида в растворе. Раствор хлорида помещают в мерную колбу на 100 мл, доводят дистиллированной водой до метки и перемешивают. Для титрования отбирают в коническую колбу 10 мл полученного раствора, немного разбавляют водой, добавляют 0.5 мл раствора К2СгO4 и титруют раствором АgNОз до изменения окраски содержимого колбы из лимонно-желтой в желто-розовую. Рассчитывают содержание хлора в полученном растворе (в граммах).
Источник
Аргенометрия. Методы Мора и Фольгарда.
Аргенометрия-метод объемного анализа, основанный на применении стандартного раствора нитрата серебра. Различают несколько методов аргенометрии: метод просветления, метод Мора, метод Фольгарда, метод Фаянса.
Метод Мора применяется для определения бромидов и хлоридов. Он основан на реакции, протекающей между Ag + и Cl — ,выполняется в присутствии индикатора – раствора хромата калия. Лишняя капля титрованного раствора AgNO3, прибавленная после достижения точки эквивалентности, вызывает выпадение кирпично-красного осадка Ag2CrO4, образующегося в результате взаимодействия Ag + с ионами индикатора: 2Ag + +CrO4 -2 =Ag2CrO4. Этот метод выполняется только в нейтральной или слабощелочной среде. В сильнощелочной среде образуется AgOH, который сразу же распадается на Ag2O и H2O: 2Ag + OH — =Ag2O+H2O.
Метод Фольгарда, основанный на реакции, протекающей между Ag + и SCN — , выполняется в присутствии индикатора- насыщенного раствора железлоаммонийных квасцов, содержащих ионы железа. Ag + +SCN — =AgSCN.
Лишняя капля раствора NH4SCN, прибавленная после достижения точки эквивалентности, вызывает появление кроваво-красного окрашивания раствора вследствие взаимодействия SCN — с ионами Fe +3 индикатора: Fe +3 +3SCN — =Fe(SCN)3. Этот метод применяется в нейтральной и кислой среде. В щелочной среде Fe +3 образует осадок Fe(OH)3, а Ag + может образовать осаок Ag2O.
9. Термохимические уравнения и расчеты. Закон Гесса и следствия из него. Стандартные теплоты сгорания и образования и их применение для термохимических расчетов.
Уравнения химических реакций, в которых записывается величина теплового эффекта, называются термохимическими. Для определения теплового эффекта используется калориметр, снабженный точным термометром. Количество теплоты, выделяющейся в калориметре, определяют по общей теплоемкости всех частей калориметра и изменению температуры: Q=C∆t, С=m1c1+m2c2.
Закон Гесса гласит: тепловой эффект реакции зависит только от природы и состояния исходных веществ и конечных продуктов и не зависит от пути, по которому реакция протекает.
1 следствие из закона Гесса: тепловой эффект реакции равен сумме теплот образования продуктов реакции минус сумма теплот образования исходных веществ.
2 следствие из закона Гесса: тепловой эффект реакции равен сумме теплот сгорания исходных веществ минус сумма теплот сгорания продуктов реакции.
Стандартной теплотой образования называется тепловой эффект образования 1 моль сложного вещества из простых веществ при стандартных условиях.
Стандартной теплотой сгорания называется тепловой эффект сгорания 1 моль органического вещества до Co2 и H2O при стандартных условиях, а если речь идет о неорганических веществах, то указываются степени окисления продуктов сгорания.
Обратимые и необратимые по направлению реакции. Понятия о химическом равновесии. Принцип Ле-Шателье.
Состояние реагирующих веществ, при котором скорость прямой реакции равна скорости обратной реакции называется состоянием химического равновесия. Состояние химичесчкого равновесия характеризуется константой равновесия K. Так, для реакции H2+I2=2HI
K=
Для обратимой реакции
В 1884г. Французский ученый Ле-Шателье сформулировал принцип подвижного равновесия: при изменении каких-либо параметров системы, находящейся в химическом равновесии, происходит смещение его в направлении, при котором уменьшается влияние этого изменения.
Химическая кинетика, как основа для изучения скоростей и механизма биохимических процессов. Средняя скорость реакции.
Кинетика-наука, изучающая механизм и закономерности протекания химических реакций. В хим.кинетике используется графический метод изображения функциональных зависимостей.
Vср.= 


Скоростью химической реакции называется изменение концентрации реагирующих веществ в единицу времени.
Vср.=lim( 



Источник
2.8.1. Аргентометрический метод (метод Мора)
Метод основан на титровании хлоридов в нейтральной среде раствором нитрата серебра в присутствии индикатора хромата калия.
Метод предназначен для определения массовой доли соли в полуфабрикатах, в которых нормируется этот показатель, а также в блюдах (изделиях) в случае разногласий при органолептической оценке.
Аппаратура, материалы, реактивы. Весы лабораторные; мясорубка бытовая; аппарат для встряхивания; термометр ртутный стеклянный со шкалой до 100 °C с ценой деления 1 °C; бюретки вместимостью 10, 25 куб. см; стаканы химические вместимостью 50, 100, 300, 400 куб. см; колбы мерные вместимостью 250 куб. см; колбы конические 100, 250 куб. см; пипетки вместимостью 10, 25, 50 куб. см; тигли фарфоровые; воронки стеклянные; бумага фильтровальная; вата гигроскопическая; палочка стеклянная; нитрат серебра, раствор концентрацией 0,05 моль/куб. дм; хромат калия, раствор с массовой долей 10% или насыщенный гидроксид натрия или калия, раствор концентрацией 0,1 моль/куб. дм (0,1 н); азотная кислота, раствор с массовой долей 10%; фенолфталеин, спиртовой раствор с массовой долей 1%; бумага индикаторная универсальная; вода дистиллированная.
Приготовление испытуемого раствора (водной вытяжки). Величину навески (m, г) рассчитывают по формуле:
a — заданная массовая доля соли в растворе, который используется для титрования, % (0,2 — 0,5%);
V — объем мерной колбы, в которую перенесена навеска;
в — предполагаемая массовая доля соли в блюде (изделии), % (для нормально посоленных блюд в зависимости от их вида массовая доля соли составляет от 0,8 до 1,2%, пересоленных — выше 1,2% до 3%).
Массовую долю поваренной соли в блюдах (изделиях) определяют в пробах, подготовленных к анализу, как указано в разделе 4.
При исследовании кулинарных изделий из натурального жареного мяса пробу после удаления костей и сухожилий два раза измельчают в мясорубке с диаметром отверстий решетки 3 — 4,5 мм и тщательно перемешивают. Пробы студней и изделий из рубленого мяса измельчают в мясорубке один раз и тщательно перемешивают.
Из подготовленной пробы блюда (изделия) отбирают навеску и взвешивают с точностью до 0,01 г в химическом стакане или фарфоровой чашке, приливают 40 — 50 куб. см горячей (70 — 80 °C) дистиллированной воды, хорошо размешивают продукт стеклянной палочкой и количественно, без потерь, переносят при помощи воронки в мерную колбу вместимостью 200 — 250 куб. см, смывая прилипшие частицы навески водой.
Колбу доливают дистиллированной водой до половины объема, закрывают пробкой и помещают в аппарат для встряхивания на 15 мин. При отсутствии аппарата для встряхивания содержимое колбы настаивают 25 — 30 мин., периодически взбалтывая.
В связи с тем, что хромат серебра растворяется в кислотах, метод Мора применим лишь в нейтральной или слабощелочной среде, поэтому после охлаждения содержимого до комнатной температуры проверяют реакцию среды по универсальной индикаторной бумаге и при наличии кислот их нейтрализуют 0,1 моль/куб. дм (0,1 н) раствором щелочи в присутствии фенолфталеина. Далее колбу доливают дистиллированной водой до метки, закрывают пробкой, содержимое колбы хорошо перемешивают и фильтруют через сухой складчатый фильтр или вату в сухой стакан или колбу. Нейтрализацию водной вытяжки можно провести непосредственно перед титрованием в конической колбе, отобрав аликвотную часть.
Можно также использовать водную вытяжку, приготовленную для определения общей кислотности. В этом случае определенное количество фильтрата, взятое для титрования, предварительно нейтрализуют 0,1 моль/куб. дм (0,1 н) раствором щелочи в присутствии фенолфталеина.
Проведение испытания. В зависимости от предполагаемого содержания соли 10 — 50 куб. см фильтрата пипеткой переносят в коническую колбу; при наличии кислот фильтрат нейтрализуют 0,1 моль/куб. дм (0,1 н) раствором щелочи в присутствии фенолфталеина, приливают 6 — 8 капель 10-процентного или 1 — 2 капли насыщенного раствора хромата калия и титруют 0,05 моль/куб. дм (0,05 н) или 0,1 моль/куб. дм (0,1 н) раствором нитрата серебра при энергичном взбалтывании до появления в колбе красно-бурого осадка.
При исследовании бульонов 20 куб. см бульона титруют 0,05 моль/куб. дм (0,05 н) раствором нитрата серебра.
При определении содержания хлорида натрия в кулинарных полуфабрикатах или изделиях из рыбы или в пробах с интенсивной окраской, затрудняющей титрование, навеску рекомендуется озолять. Для этого в тигель берут навеску, подсушивают ее в сушильном шкафу при постепенном повышении температуры до 120 — 140 °C. Высушенную массу осторожно обугливают на газовой горелке до получения остатка темно-серого цвета, легко распадающегося при надавливании стеклянной палочкой. Затем обугленную массу осторожно измельчают палочкой, обрабатывают 4 — 5 раз небольшими порциями горячей воды (80 — 90 °C), каждый раз сливая жидкую часть посредством стеклянной палочки на бумажный фильтр. Фильтрат собирают в мерную колбу вместимостью 250 куб. см. Остаток в тигле и на фильтре промывают горячей водой до прекращения реакции последних порций фильтрата с нитратом серебра. Для этого небольшую порцию (1 — 2 куб. см) фильтрата подкисляют в пробирке 1 — 2 каплями раствора азотной кислоты с массовой долей 10% и прибавляют 1 — 2 капли раствора нитрата серебра. Если фильтрат остается прозрачным, обработку золы горячей водой заканчивают. При необходимости фильтрат в мерной колбе нейтрализуют раствором щелочи в присутствии фенолфталеина, доводят водой до метки, закрывают пробкой и хорошо перемешивают.
Обработка результатов. Массовую долю хлорида натрия (Х) в процентах или в граммах в блюде (изделии) рассчитывают по формуле:
Расхождение между результатами параллельных определений не должно превышать 0,02%.
За конечный результат принимают среднее арифметическое двух параллельных определений, вычисленное с точностью до 0,1%.
Источник