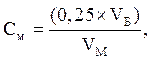- Раствор соли Мора (0,25 н.), титрованный
- ГОСТ 25794.2-83 Реактивы. Методы приготовления титрованных растворов для окислительно-восстановительного титрования
- Способы доставки
- Оглавление
- Этот ГОСТ находится в:
- Организации:
- Reagents. Methods of preparation of standard volumetric solutions for redox titrimetry
- РЕАКТИВЫ
Раствор соли Мора (0,25 н.), титрованный
Раствор соли марганца
Раствор серной кислоты (1:15) для перманганатной окисляемости
1 объем концентрированной серной кислоты квалификации не хуже «ч.д.а» медленно, при постоянном перемешивании, отводя выделяющееся тепло (Техника безопасности!)добавляют к 14 объемам дистиллированной воды в подходящей посуде. К теплому (температура 40 °С) раствору по каплям добавляют 0,01 н. раствор перманганата до стабильного бледно-розового оттенка.
Раствор серной кислоты (10%)
В мерную колбу вместимостью 100 мл помещают 20-30 мл дистиллированной воды. Туда же постепенно, при перемешивании, добавляют пипеткой 5,4 мл концентрированной серной кислоты. (Техника безопасности!).Раствор перемешивают покачиванием и добавляют дистиллированную воду до метки 100 мл.
Раствор приготавливают в подходящей посуде из 4-водного сульфата марганца (концентрация 480 г/л) либо 4-водного хлорида марганца (концентрация 425 г/л) в дистиллированной воде.
В мерную колбу вместимостью 1 л помещают 49,0 г соли Мора (NH4)2Fe(SO4)2×6H2O и 100-150 мл дистиллированной воды. Туда же осторожно добавляют при перемешивании 10 мл концентрированной серной кислоты (Техника безопасности!), после чего доводят объем раствора дистиллированной водой до 1 л. Хранят раствор в плотно закрытой посуде не более 6 мес.
Титр (точную концентрацию) этого раствора устанавливают по раствору бихромата калия (0,25 н.) перед серией определений. Для этого в коническую колбу на 500 мл помещают 25 мл раствора бихромата, добавляют 225 мл дистиллированной воды и 20 мл концентрированной серной кислоты (Техника безопасности!). Раствору дают остыть, после чего пипеткой-капельницей к нему прибавляют 3-4 капли раствора индикатора ферроина и титруют раствором соли Мора.
Титр раствора соли Мора в г-экв/л рассчитывают по формуле:
где: 0,25 – концентрация раствора бихромата калия, г-экв/л;
VБ и VM – объемы растворов: взятого для титрования раствора бихромата и израсходованного на титрование раствора соли Мора, мл.
Раствор соляной кислоты (0,05 г-экв/л)
Раствор приготавливают из фиксанала, используя дистиллированную воду.
Раствор соляной кислоты (1:10)
К 10 мл дистиллированной воды постепенно при перемешивании добавляют 1 мл концентрированной соляной кислоты. (Техника безопасности!).
Раствор солянокислого гидроксиламина (10%)
10,0 г солянокислого гидроксиламина (NH2OH•HCl) растворяют в
90 мл дистиллированной воды.
Раствор тиосульфата натрия (ОД г-экв/л и 0,02 г-экв/л)
Приготавливаются из ампулы фиксанала (стандарт-титра) тиосульфата натрия («0,1 г-экв/л»).
Для приготовления раствора тиосульфата с концентрацией 0,1 г-экв/л содержимое ампулы количественно переносят в мерную колбу на 1000 мл. Туда же добавляют 200-300 мл свежепрокипяченной и охлажденной дистиллированной воды. Тиосульфат растворяют в указанном количестве воды, после чего объем раствора в мерной колбе доводят до метки такой же дистиллированной водой. Приготовленного раствора тиосульфата достаточно для выполнения 1000 и более анализов.
Для приготовления 0,02 г-экв/л раствора тиосульфата 20,0 мл раствора с концентрацией 0,1 г-экв/л, отмеренные с помощью цилиндра, помещают в мерную колбу на 100 мл, после чего объем раствора в мерной колбе доводят до метки дистиллированной водой.
Для повышения стабильности растворов тиосульфата к ним следует добавить 10 мл амилового или изобутилового спирта (либо 1-2 мл ксилола или хлороформа) на 1 л раствора.
Растворы используют не ранее чем через 10 дней после приготовления.
В процессе использования раствора следует периодически (например, перед началом полевых работ) устанавливать точную концентрацию стандартного раствора тиосульфата методом титрования раствором бихромата калия.
Раствор трилона Б (0,05 г-экв/л)
Раствор приготавливают из фиксанала, используя дистиллированную воду.
Раствор хромата калия (10%)
10,0 г К2СrO4 растворяют в 90 мл дистиллированной воды.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
ГОСТ 25794.2-83
Реактивы. Методы приготовления титрованных растворов для окислительно-восстановительного титрования
Купить ГОСТ 25794.2-83 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО «ЦНТИ Нормоконтроль»
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на реактивы и устанавливает методы приготовления следующих титрованных растворов для окислительно-восстановительного титрования и методы проверки их молярной концентрации.
Издание (май 2008 г.)
Оглавление
1 Общие указания
2 Приготовление титрованных растворов
| Дата введения | 01.07.1984 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Актуализация | 01.02.2020 |
Этот ГОСТ находится в:
- Раздел Электроэнергия
- Раздел 71 ХИМИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ
- Раздел 71.040 Аналитическая химия
- Раздел 71.040.30 Химические реактивы
- Раздел 71.040 Аналитическая химия
- Раздел 71 ХИМИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ
- Раздел Экология
- Раздел 71 ХИМИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ
- Раздел 71.040 Аналитическая химия
- Раздел 71.040.30 Химические реактивы
- Раздел 71.040 Аналитическая химия
- Раздел 71 ХИМИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ
Организации:
| 23.05.1983 | Утвержден | Госстандарт СССР | 2303 |
|---|---|---|---|
| Разработан | Министерство химической промышленности СССР | ||
| Издан | Издательство стандартов | 1983 г. | |
| Издан | ИПК Издательство стандартов | 2001 г. | |
| Издан | ИПК Издательство стандартов | 2003 г. | |
| Издан | Стандартинформ | 2008 г. |
Reagents. Methods of preparation of standard volumetric solutions for redox titrimetry
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:
РЕАКТИВЫ
МЕТОДЫ ПРИГОТОВЛЕНИЯ ТИТРОВАННЫХ РАСТВОРОВ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОГО ТИТРОВАНИЯ
МЕТОДЫ ПРИГОТОВЛЕНИЯ ТИТРОВАННЫХ РАСТВОРОВ ДЛЯ ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОГО ТИТРОВАНИЯ
Methods of preparation of standard volumetric solutions for redox titration
M КС 71.040.30 ОКСТУ 2609
Дата введения 01.07.84
Настоящий стандарт распространяется на реактивы и устанавливает методы приготовления следующих титрованных растворов для окислительно-воссгановительного титрования it методы проверки их молярной концентрации:
аммоний ванадиевокислый мета, растворы молярных концентраций: с (NH4VO,) = 0.1 моль/дм 3 (0.1 н.); c(NH4VO,) = 0.05 моль/дм 3 3 (0.1 н.); йод. раствор молярной концентрации: с О/2 -Ы = 0.1 моль/дм 3 (0.1 н.);
калий бромноватокислый, раствор молярной концентрации: с(‘/6 KBrOj) = 0.1 моль/дм 3 (0.1 н.); калий двухромовокислый, раствор молярной концентрации: с 0/6 К2Сг207) = 0.1 моль/дм 3 (0.1 н.);
калий железосинеродистый, раствор молярной концентрации: с (KjFe(CN6) = 0.05 моль/дм 3 (0,05 н.); калий йодноватокислый, растворы молярных концентраций: с (КЮД = 0.1 моль/дм 3 ; с 0/ь KJO,) = 0.1 моль/дм 3 ; с ( l /5 KJO,) = 0,1 моль/дм 3 ;
калий марганцовокислый, раствор молярной концентрации: с (*/5 КМп04) = 0,1 моль/дм 3 (0.1 н.); кислота щаве;1евая. раствор молярной концентрации: с (У2 Н2С204 2Н20) = 0.1 моль/дм 3 (0.1 н.):
мышьяк (III) окись (мышьяковистый ангидрид), раствор концентрации: с ( l /4 As20,) = 0.1 моль/дм 3 (0.1 н.);
натрий серноватистокислый, раствор молярной концентрации:
церий (IV) сульфат, растворы молярных концентраций:
I. ОБЩИЕ УКАЗАНИЯ
И здание официальное
1.1. Общие указания — но ГОСТ 25794.1
© Издательство стандартов. 1983 © СТАНДАРТИНФОРМ. 2008
2. ПРИГОТОВЛЕНИЕ ТИТРОВАННЫХ РАСТВОРОВ
2.1. Аммоний нанадисвокислый мета, раствор молярной концентрации с (NII4VO,) ■ = 0,1 моль/дм’
Относительная молекулярная масса — 116.98.
Молярная масса эквивалента — 116.98 г/моль.
2.1.1. Реактивы и растворы
Аммоний ванадиевокислый мета по ГОСТ 9336.
Дифениламин по ТУ 6—09—5467. раствор с массовой долей I %.
Натрий N-фенилсульфанилат (индикатор), раствор с массовой долей 0,5 %.
Кислота серная по ГОСТ 4204.
Кислота ортофосфорная но ГОСТ 6552.
Кислота N-фенилантрониловая но ТУ 6—09—3592. раствор с массовой долей 0.1 %.
Смесь кислот, готовят следующим образом: к 300 см 3 воды добавляют при перемешивании 100 см’ серной кислоты и посте охлаждения 100 см’ ортофосфорной кислоты.
Соль закиси железа и аммония двойная сернокислая (соль Мора) по 1’ОСТ 4208. раствор молярной концентрации с (NH4)2S04 FeS04 6Н20) = 0.1 моль/дм 3 , приготовленный по и. 2.2.
2.1; 2.1.1. (Измененная редакция, Изм. № 1).
2.1.2. Приготовление растворов
11.70 г (для раствора 0.1 моль/дм 3 ) или 5.85 г (для раствора 0.05 моль/дм 3 ) ванадиевокислого аммония мета растворяют в смеси, состоящей из 200 см’ воды и 150 см’ серной кислоты, при энергичном перемешивании. Посте растворения препарата раствор охлаждают и доводят объем раствора водой до 1 дм 3 .
2.1.3. Определение коэффициента поправки
25—35 см’ раствора соли Мора, отмеренные бюреткой, помещают в коническую колбу вместимостью 500 см’, добавляют 50 см 3 смеси кислот, 100 см 3 воды, 2—3 капли раствора N-фенилсульфанилата натрия и медленно при тщательном перемешивании титруют из бюретки приготовленным раствором ванадиевокислого аммония мета до перехода окраски в сине-фиолетовую.
Допускается проводить титров;»ние в присутствии 2—3 капель раствора N-фенилантраниловой кислоты до перехода окраски в вишнево-красную или в присутствии 5 капель раствора дифениламина до перехода окраски в сине-фиолетовую.
2.2. Соль закиси железа и аммония двойная сернокислая (соль Мора), раствор молярной концентрации с (NH4)2S04 FeS04 6Н20) = 0,1 моль/дм 3 (0,1 и.)
Относительная молекулярная масса — 392.13.
Молярная масса эквивалента — 392.13 г/моль.
2.2.1. Реактивы и растворы
Вода диспыл про ванная, не содержащая кислорода.
Калий марганцовокислый по ГОСТ 20490. раствор молярной концентрации с 0/$ КМп04) = = 0.1 моль/дм 3 (0.1 н.). приготовленный по и. 2.8.
Калий двухромовокислый по ГОСТ 4220. раствор молярной концентрации с ( 1 / 3 (0,1 н.). приготовленный по и. 2.5.
Кислота серная по ГОСТ 4204.
Кислота ортофосфорная по ГОСТ 6552.
Кислота N-фенилантраниловая, раствор с массовой долей I %.
Соль закиси железа и аммония двойная сернокислая (соль Мора) по ГОСТ 4208.
2.1.3—2.2.1. (Измененная редакция. Изм. № I).
2.2.2. Приготовление раствора
40.00 г соли Мора растворяют в смеси, состоящей из 200 см’ воды и 30 см’ серной кислоты, и доводят объем раствора водой до 1 дм 3 (если необходимо, раствор фильтруют). Коэффициент поправки устанавливают в день применения.
2.2.3. Определение коэффициента поправки по раствору марганцовокислого калия
25—35 см 3 раствора соли Мора, отмеренные бюреткой, помещают в коническую колбу вместимостью 250 см’, добавляют 5 см’ ортофосфорной кислоты и титруют из бюретки раствором марганцовокислого калия до появления не исчезающей в течение 30 с розовой окраски.
При необходимости в результат определения вносят поправку, устанавливаемую контрольным опытом.
(Измененная редакция. Изм. № 1).
2.2.4. Определение коэффициента поправки по раствору двухромовокислого калия
25—30 см* раствора соли Мора, отмеренные бюреткой, помешают в коническую колбу вместимостью 500 см 3 . прибавляют 250 см 3 воды, не содержащей кислорода. 10 см 3 серной кислоты,
0.5 см 3 раствора N-фенил антраниловон кислоты и титруют из бюретки раствором двухромово кисло го калин до появлении вишне во-крас ной окраски раствора.
(Введен дополнительно, Изм. № 1).
2.3. Йод, раствор молярной концентрации с (*/2 .12) = 0,1 моль/дм 3 (0,1 н.)
Относительная молекулярная масса — 253.80.
Молярная масса эквивалента — 126.90 г/моль.
2.3.1. Реактивы и растворы
Калий йодистый но ГОСТ 4232.
Кислота серная но ГОСТ 4204. раствор с массовой долей 25 %.
Крахмал растворимый по ГОСТ 10163, растворе массовой долей 0,5 %.
Натрий серноватистокислый (натрия тиосульфат) 5-водный но ГОСТ 27068. раствор молярной концентрации с (Na2S20,5H20) * 0.1 моль/дм 3 (0.1 н.). приготовленный по п. 2.11.
2.3.2. Приготовление раствор;!
12.70 г йода растворяют в 60 см 3 воды, содержащих 40 г йодистого калия, и тщательно перемешивают до папюго растворения йода. Затем объем раствора доводят водой до 1 дм 3 . Раствор сохраняют в склянке из темного стекла с пришлифованной пробкой. Коэ фициент поправки устанавливают не реже одного раз;! в 10 суг.
Допускается готовить раствор с 25 г йодистого калия, но при этом коэффициент поправки определяют не реже одного раз;! в 2 сут.
2.3.3. Определение коэффициента поправки
30—40 см 3 раствора йода, отмеренные бюреткой, помешают в коническую колбу (с пришлифованной пробкой) вместимостью 250 см 3 , прибавляют около 25 см 3 воды, 5 см 3 раствора серной кислоты и титруют из бюретки раствором 5-водного серноватистокислого натрия до перехода бурой окраски раствора и соломенно-желтую. Затем прибавляют 2 см 3 раствор;! крахмала и продолжают титрование при тщательном перемешивании до обесцвечивания раствора.
Допускается определять коэффициент поправки по окиси мышьяка (III) по п. 2.10.3 раствором точной молярной концентрации, приготовленным по и. 2.10.4.
2.4. Калий брочноватокислый, раствор молярной концентрации с (‘/6 КВЮ,) ■ 0.1 моль/дм 3 (0,1 н.)
Относительная молекулярная масса — 167.00.
Молярная масса эквивалента — 27.83 г/моль.
2.4.1. Реактивы и растворы
Калий бромистый по ГОСТ 4160.
Калий бромноватокислый но ГОСТ 4457.
Калий йодистый по ГОСТ 4232. раствор с массовой долей 30 % свежеприготовленный.
Кислота серная но ГОСТ 4204, раствор с массовой долей 20 %.
Крахмал растворимый по ГОСТ 10163. растворе массовой долей 0.5 %.
Натрий серноватистокислый (натрия тиосульфат) 5-водный по ГОСТ 27068. раствор молярной концентрации с (Na2S20,5H20) = 0.1 моль/дм 3 (0.1 н.). приготовленный по и. 2.11.
2.3—2.4.1. (Измененная редакция. Изм. № 1).
2.4.2. Приготовление раствор;!
10.00 г бромистого калии и 2.78 г бромноватокислого калии растворяют в воде и доводят объем раствора водой до 1 дм 3 .
2.4.3. Определение коэффициента поправки
30—40 см 3 раствор;! бромноватокислого калии, отмеренные бюреткой, помешают в коническую колбу вместимостью 500 см 3 с пришлифованной пробкой, прибавляют 10 см 3 раствора йодистого калия. 20 см 3 раствора серной кислоты, сразу закрывают колбу пробкой, смоченной раствором йодистого калии, затем перемешивают и выдерживают в темноте в течение 10 мин. после чего
пробку и стенки колбы обмывают кодой и выделившийся йод титруют из бюретки раствором 5-водного серноватистокислого натрия до перехода окраски раствора в соломенно-желтую, затем добавляют 2 см’ раствора крахмала и продолжают титрование при тщательном перемешивании до обесцвечивания раствора.
При необходимости в результат определения вносят поправку, устанавливаемую контрольным опытом.
2.5. Калий двухромовокислый, раствор молярной концентрации с (‘/6 К,(‘г,О.) — 0.1 моль/дм’
Относительная молекулярная масса — 294.18.
Малярная масса эквивалента — 49.03 г/моль.
2.5.1. Реактивы и растворы
Калий двухромовокислый но ГОСТ 4220.
Калий двухромовокислый с массовой долей основного вещества (100,0±0,2) % или дважды перекристаллизованный из воды (растворимость в 100 см’ воды при 20 ’С — 12.3 г. при 100 *С — 103 г) и после измельчения высушенный при 150 *С до постоянной массы или стандартный образец калия двухромовокислого для титриметрии ГСО I разряда № 2215—81 или ГСО II разряда.
Калий йодистый по ГОСТ 4232. раствор с массовой долей 30 % свсжеприютовленныи.
Крахмал растворимый по ГОСТ 10163. растворе массовой далей 0,5 %.
Кислота серная по ГОСТ 4204, раствор с массовой далей 20 %.
Натрий серноватистокислый (натрия тиосульфат) 5-водный но ГОСТ 27068. раствор малярной концентрации с (Na2S20v5H20) = 0.1 моль/дм’ (0.1 н.). приготовленный по п. 2.11.
(Измененная редакция, Изм. № 1).
2.5.2. Приготовление раствора
4.90 г двухромовокислого калия растворяют в воде и доводят объем раствора водой до 1 дм’.
2.5.3. Определение коэффициента поправки
30—40 см’ раствора двухромовокислого калия, отмеренные бюреткой, помещают в коническую колбу вместимостью 500 см’ с пришлифованной пробкой, прибавляют 10 см’ раствора йодистого калия. 20 см’ раствора серной кислоты, сразу закрывают колбу пробкой, смоченной раствором йодистого калия, перемешивают и выдерживают в течение 10 мин в темноте, после этою обмываю! пробку и стенки ка1бы водой, прибавляют 200 см’ воды и титруют выделившийся йод из бюретки раствором 5-водного серноватистокислого натрия до изменения цвета раствора в желтый, затем прибавляют 2 см’ раствора крахмала и продолжают титрование при тщательном перемешивании до перехода синей окраски в светло-зеленую.
При необходимости в результат определения вносят поправку, устанавливаемую контрольным опытом.
2.5.4. Приготовление раствора точной молярной концентрации
4.9031 г двухромовокислого калия (с массовой долей основного вещества (100.0±0,2) % или пере кристаллизованного) или стандартного образца двухромовокислого калия для титриметрии ГСО I разряда № 2215—81 или ГСО II разряда растворяют в воде в мерной колбе вместимостью I дм’ и доводят объем раствора водой до метки.
2.6. Калий железосинеролистый, раствор молярной концентрации с (K,Fe (CN)6— в 0,05 моль/дм 3 (0,05 н.)
Относительная молекулярная масса — 329.25.
Молярная масса эквивалента — 329,25 г/моль.
2.6.1. Реактивы и растворы
Калий железосинеродистый по ГОСТ 4206 и перекристаллизованный из воды, измельченный и высушенный при 105—110 *С до постоянной массы.
Калий йодистый по ГОСТ 4232. раствор с массовой далей 30 %. свежеприготовленный.
Крахмал растворимый по ГОСТ 10163, растворе массовой долей 0,5 %.
Натрий серноватистокислый (натрия тиосульфат) 5-водный по ГОСТ 27068. раствор малярной концентрации с (Na2S20,5Н20) = 0.05 моль/дм’ (0.05 н.), приготовленный по п. 2.11 с соответствующим изменением навески.
Цинк сернокислый 7-водный по ГОСТ 4174. растворе массовой далей 10 %.
2.6.2. Приготовление раствора
16,50 г железосинеродистого калия растворяют в воде и доводят объем раствора водой до 1 дм 3 .
Раствор хранят в склянке из темною стекла. Коэффициент поправки раствора определяют не реже одного pa w в 10 сут.
2.6.3. Определение коэффициента поправки
30—40 см ‘ раствора железосинеродистого калия, отмеренные бюреткой, помешают в коническую колбу вместимостью 500 см 3 с пришлифованном пробкой, прибавляют 30 см 3 раствора 7-вод-ного сернокислого цинка, 10 см 3 раствора йодистого калия, закрывают колбу пробкой, смоченной раствором йодистого калия, тщательно перемешивают и выдерживают в темноте в течение 10 мин. после чего обмывают пробку и стенки колбы небольшим объемом воды и титруют из бюретки раствором 5-водного серноватистокислого натрия до перехода окраски раствора в соломенно-желтую. Затем прибавляют 2 см 3 раствора крахмала и продолжают титрование медленно при тщательном перемешивании до обесцвечивания раствора.
При необходимости в результат определения вносят поправку, устанавливаемую контрольным опытом.
2.6.4. Приготовление раствора точной молярной концентрации
16.4624 г перекриста/тлизованного железосинеродистого калия растворяют в воде в мерной колбе вместимостью 1 дм 3 и доводят объем раствора водой до метки.
2.7. Калий йодноватокислый. растворы молярных концентраций
с (KJO*) = 0.1 моль/дм 3 . с ( ! /б KJO,) = 0.1 моль/дм 3 , с (7S KJO,) = 0.1 моль/дм 3 .
Относительная молекулярная масса — 214.00.
Молярная масса эквивалента соответственно 21.40; 3.57; 4.28 г/моль.
2.5.3—2.7. (Измененная редакция, Изм. № I).
2.7.1. Реактивы и растворы
Калий йодноватокислый по ГОСТ 4202 перекристгилизованный из воды и высушенный при 120—150 *С до постоянной массы.
2.7.2. Приготовление раствора точной молярной концентрации
В воде в мерной колбе вместимостью 1 дм 3 растворяют следующие массы перекристаллизо-ва иного йодновато кислого калия:
для раствора молярной концентрации с (KJO,)= 0.1 моль/дм 3 — 21.4000 г; для раствора молярной концентрации с (7« KJO,) = 0.1 моль/дм 3 — 3.5667 г; для раствора молярной концентрации с (•/* KJO,) = 0.1 моль/дм 3 — 4.2800 г.
Объемы растворов доводят водой до метки.
2.8. Калий марганцовокислый, раствор молярной концентрации с(*/5 КМо04) = 0.1 моль/дм 3 (0,1 и.)
Относительная молекулярная масса — 158.03.
Молярная масса эквивалента — 31,60 г/моль.
2.8.1. Реактивы, растворы и посуда
Калий йодистый по ГОСТ 4232. раствор с массовой долей 30 %. свежеприготовленный. Калий марганцовокислый по ГОСТ 20490.
Кислота серная по ГОСТ 4204. концен трированная и раствор с массовой долей 20 %. Крахмал растворимый по ГОСТ 10163. растворе массовой долей 0.5 %.
Натрий серноватистокислый (натрия тиосульфат) 5-водный по ГОСТ 27068. раствор молярной концентрации с (Na2S20,5H20) — 0.1 моль/дм 3 (0.1 н.). приготовленный по п. 2.11.
Натрий щавелевокислый по ГОСТ 5839. высушенный при 100—105 *С до постоянной массы. Воронка типа ВФ-1 (2) ПОРЮ или ВФ-К2) ПОР16 по ГОСТ 25336.
2.8.2 Приготовление раствора
3.25 г марганцовокислого калия растворяют в воде, доводят объем раствора до I дм 3 и выдерживают в течение 20 сут. Затем раствор фильтруют через стеклянную воронку.
Допускается более быстрый способ приготовления раствора: 3.25 г марганцовокислого калия растворяют в 900 см 3 воды в колбе вместимостью I дм 3 . Раствор назревают приблизительно до 80 ’С. накрыв колбу, выдерживают при этой температуре в течение 2 ч, а затем выдерживают в течение I сут при комнатной температуре, после этого раствор фильтруют через стеклянную воронку.
Раствор хранят длительное время в склянке из темного стекла. Следует избегать соприкосновения раствора марганцовокислого калия с резиновыми трубками или пробками; при титровании необходимо пользоваться бюретками со стеклянными кранами.
2.7.2—2.8.2. (Измененная редакция, Изм. № 1).
2.8.3. Определение коэффициента поправки
2.8.3.1. Определение коэффициента поправки но щавелевокислому натрию
Относительная молекулярная масса — 134,00.
Молярная масса эквивалента — 67.00 г/моль.
0.1500—0.2500 г щавелевокислого натрия помешают в коническую колбу вместимостью 250 см 3 , растворяют в 50 см 3 воды, прибавляют 8 см 3 серной кислоты, шнревают до 70—80 *С и титруют из бюретки раствором марганцовокислого калия. При этом титрование сначала проводят очень медленно, не прибавляя последующей капли, пока предыдущая наш остью нс обесцветится. В конце титрования титруют быстрее до появления не исчезающей в течение 1 мин розовой окраски раствора.
Температура раствора в конце титрования должна быть не менее 60 ‘С.
При необходимости в результат определения вносят поправку, устанавливаемую контрольным опытом.
2.8.3.2. Определение коэффициента поправки но раствору 5-водного ссрноватистокислого натрия
30—40 см 3 раствора марганцовокислого калия, отмеренные бюреткой, помещают в коническую колбу вместимостью 500 см 3 с пришлифованной пробкой, прибавляют 10 см 3 раствор;» йодистою калия, 20 см 3 раствора серной кислоты с массовой далей 20 %, сразу закрывают колбу пробкой, смоченной раствором йодистого калия, затем перемешивают и выдерживают в темноте в течение 10 мин. после чего обмывают пробку и стенки калбы водой, прибавляют 200 см 3 воды и выделившийся йод титруют из бюретки раствором 5-водного серноватистокислого натрия до перехода окраски раствора в соломенно-желтую, затем прибавляют 2 см 3 раствора крахмала и продолжают титрование при тщательном перемешивании до обесцвечивания раствор;».
При необходимости в результат определения вносят поправку, устанавливаемую контрольным опытом.
2.8.3.1. 2.8.3.2. (Измененная редакция, Изм. Ns 1).
2.8.3.3. (Исключен, Изм. Ns 1).
2.9. Кислота щавелевая, раствор молярной концентрации с (*/2 Н2С204 2Н20) =0,1 моль/дм’ (0,1 н.)
Относительная молекулярная масса — 126.07.
Машрная масса эквивалента — 63.03 г/моль.
2.9.1. Реактивы и растворы
Кисюта серная по ГОСТ 4204.
Кислота щавелевая по ГОСТ 22180.
Калий марганцовокислый по ГОСТ 20490. раствор молярной концентрации с (‘Д КМп04) = = 0.1 моль/дм 3 (0.1 н.), приготовленный по и. 2.8.
2.9.2. Приготовление раствора
6.30 г щавелевой кислоты растворяют в воде и объем раствора доводят водой до 1 дм 3 . Раствор хранят в склянке из темного стекла.
2.9.3. Определение коэффициента поправки
25—40 см’ раствора щавелевой кислоты, отмеренные бюреткой, помещают в коническую колбу вместимостью 250 см 3 , прибавляют 30 см 3 воды. 8 см’ серной кислоты, нагревают до 70—80 ’С и титруют из бюретки раствором марганцовокислого калия (как указано в и. 2.8.3.1).
При необходимости в результат определения вносят поправку, устанавливаемую контрольным опытом.
2.10. Мышьяк (III) окись, раствор малярной концсшрации с (‘/4 As20,) = 0,1 моль/дм 3 (0,1 и.)
Относительная молекулярная масса — 197.84.
Малярная масса эквивалента — 49.46 г/моль.
2.10.1. Реактивы и растворы
Йод по ГОСГ 4159. раствор молярной концентрации с (*/2 -М = 0.1 моль/дм 3 (0,1 н.). приготовленный по п. 2.3.
Кислота серная по ГОСТ 4204. раствор молярной концентрации с* (*/•» H^S04) = I моль/дм’ О н.).
Кисюта соляная по ГОСГ 3118. раствор с массовой долей 25 %.
Крахмал растворимый по ГОСТ 10163. растворе массовой долей 0.5 %.
Мышьяк (III) окись, аморфная или кристгылическая.
Мышьяк;! (III) окись, перекриспылизованная и высушенная при 105—110 ’С в течение 1—2 ч.
Натрия гидроокись по ГОСТ 4328. раствор молярной концентрации c(NaOH) = I моль/дм 3 (I н.) и раствор с массовой долей 10 %.
Натрий углекислый кислый по ГОСТ 4201.
Спирт этиловый ректификованный технический но ГОСТ 18300 высшего copra.
Фенолфталеин (индикатор) по ТУ 6—09—5360. спиртовой раствор с массовой долей 1 %.
2.10.2. Приготовление раствора
4.95 г окиси мышьяк;! (III) аморфной или кристаллической растворяют в небольшом объеме раствора гидроокиси натрия с массовой долей 10 %. Полученный раствор разбавляют водой, нейтрализуют раствором серной кислоты в присутствии раствора фенолфталеина, после чего прибавляют раствор 20 г кислого углекислого натрия в 500 см 3 воды. Если при этом появляется розовая окраска, добавляют но кашлям раствор серной кислоты до обесцвечивания раствора, после чего объем раствора доводят водой до 1 дм 3 .
2.10.3. Определение коэффициента поправки
30—40 ем 3 раствора йода, отмеренные бюреткой, помещают в коническую колбу вместимостью 500 см 3 , содержащую 200 см 3 воды, прибавляют 2 см 3 раствора соляной кислоты, затем 2 г кислого углекислого натрия. После его растворения прибавляют 3 см 3 раствора крахмала и при тщательном перемешивании титруют из бюретки раствором окиси мышьяка (III) до обесцвечивания раствора.
2.10.4. Приготовление раствора точной малярной концентрации
4.9460 г пере кристалл изованной окиси мышьяка (III) помешают в коническую калбу (или стакан) вместимостью 250 см 3 , содержащую отмеренные бюреткой 40 см 3 раствора гидроокиси натрия молярной концентрации 1 моль/дм 3 . и растворяют при н;нревании на водяной бане. После охлаждения раствор переносят в мерную колбу вместимостью I дм 3 и добавляют бюреткой 40—41 см 3 раствор;! серной кислоты. Точный необходимый объем серной кислоты вычисляют с учетом коэффициентов поправок растворов гидроокиси натрия и серной кислоты, гак как необходимо обеспечить избыток серной кислоты 0.2 см 3 , и доводят объем раствора водой до метки.
2.11. Натрий серноватистокислый. раствор молярной концентрации с (Na,S,(), 511,0) = =0.1 моль/дм 3 (0,1 н.)
Относительная молекулярная масса — 248.17.
Малярная масса эквивалента — 248.17 г/маль.
2.11.1. Реактивы и растворы
Калий двухромовокислый по ГОСТ 4220. дважды иерекристаьлизованный и высушенный по н. 2.5.1.
Калий йодистый по ГОСТ 4232. раствор с массовой далей 30 %. свежеприготовленный.
Кислота серная но ГОСТ 4204, раствор с массовой далей 20 %.
Крахмал растворимый по ГОСТ 10163, растворе массовой далей 0,5 %.
Натрий серноватистокислый (натрия тиосульфат) 5-водный по ГОСТ 27068.
Спирт изобутиловый но ГОСТ 6016.
2.11.2. Приготовление раствора
25.00 г 5-водного серноватистокислого натрия растворяют в 400 см 3 воды, прибавляют 10 см 3 изобугилового спирта, тщательно перемешивают, доводят водой объем до I дм 3 . Раствор годен к применению через 10—14 сут. Раствор хранят в склянке из темного стекла.
2.11.3. Определение коэффициента поправки
0.1500—0.2000 г двухромовокислого калия помещают в коническую колбу вместимостью 500 см 3 с пришлифованной пробкой, растворяют в 50 см 3 воды, к раствору прибавляют 10 см 3 раствора йодистого калия, 20 см 3 раствора серной кислоты, сразу закрывают колбу пробкой, смоченной раствором йодистого калия, перемешивают и выдерживают в темноте в течение 10 мин. после чего пробку и стенки колбы обмывают водой, добавляют 200 см 3 воды и выделившийся йод титруют из бюретки приготовленным раствором 5-водного серноватистокислого натрия до перехода окраски раствора в желтую, затем прибавляют 2 см 3 раствора крахмала и продалжают титрование при тщательном перемешивании до перехода синей окраски раствора в светло-зеленую.
При необходимости в результат опреле.ления вносят поправку’, устанавливаемую контрольным опытом.
2.9—2.11.3. (Изчеиенная редакция. Изм. № 1).
2.11.4. (Исключен. Изм. № 1).
2.12. Церий (IV) сульфат. растворы молярных концентраций с (0(SO^)2 4Н20) = = 0,05 моль/дм’ (0,05 н.), с (Ce(S04)2 4Н20) = 0,1 моль/дм’ (0,1 н.)
Относительная молекулярная масса — 404,29.
Молярная масса эквивалента — 404.29 г/моль.
2.12.1. Реактивы, растворы и посула
Калий йодистый но ГОСТ 4232. раствор с массовой долей 30 %. свежеприготовленный.
Кислота серная по ГОСТ 4204. концентрированная и раствор с массовой долей 20 %.
Крахмал растворимый по ГОСТ 10163. растворе массовой долей 0,5 %.
Натрий серноватнстокислый (натрия тиосульфат) 5-водный по ГОСТ 27068. раствор молярной концентрации с (Na2S20,5H20) = 0.05 моль/дм 3 (0.05 н.). приготовленный по н. 2.11 (из навески массой 12.50 г).
Натрий углекислый по ГОСТ 83.
Соль закиси железа и аммония двойная сернокислая (соль Мора) по ГОСТ 4208, раствор молярной концентрации с |(NH4)2S04FeS04-6H20) = 0.05 моль/дм 3 (0.05 н.). приготовленный по н. 2.2 (из навески массой 20.00 г).
Ферроин (индикатор), раствор. Раствор хранится длительное время.
Церий (IV) сульфат 4-водный (церий (IV)) сернокислый по ТУ 6—09—1646.
Воронка типа ВФ-1(2) ПОРЮ или ВФ-1 (2) ПОРЮ но ГОСТ 25336.
2.12.2. Приготовление растворов
20.20 г 4-волною сульфата церия (IV) для раствора 0.05 моль/дм 3 или 40.40 г для раствор;! 0.1 моль/дм 3 растворяют в I дм 3 волы, содержащем 30 см 3 концентрированной серной кислоты. Посте охлаждения, если раствор мутный, его фильтруют через стеклянную воронку типа ВФ-1 (2) ПОРЮ или ВФ-1 (2) ПОРЮ (ГОСТ 25336-82) и доводят объем раствора водой до 1 дм 3 .
Допускается применять также церий (IV) по ТУ 6—09—04—177, сульфат безводный и аммоний церий (IV) сульфат (4:1) 2-водный с изменением навески в соответствии с молекулярной массой.
2.12—2.11.2. (Измененная редакция, Изм. № I).
2.12.3 Определение коэс|н|>ициента поправки
2.12.3.1. Определение коэ фиииентл поправки но раствору 5-водного серноватистокислого натрия
30—40 см’ раствора 4-водного сульфата церия (IV). отмеренные бюреткой, помещают в коническую колбу вместимостью 500 см 3 с пришлифованной пробкой, прибавляют 10 см 3 раствора серной кислоты с массовой долей 20 %, 0.5 г углекислого натрия. 10 см 3 раствор;! йодистого калия, сразу закрывают колбу пробкой, смоченной раствором йодистого калия, перемешивают и выдерживают в темноте в течение 10 мин, после чего пробку и стенки колбы обмывают водой и выделившийся йод титруют из бюретки раствором 5-водного серноватистокислого натрия до перехода окраски в соломенно-желтую, затем прибавляют 2 см’ раствора крахмала и продолжают медленное титрование при тщательном перемешивании до обесцвечивания раствора.
2.12.3.2. 30—40 см 3 раствора соли Мора, отмеренные бюреткой, помещают в коническую колбу вместимостью 250 см’, прибавляют 1—2 капли раствора ферроина и титруют из бюретки раствором 4-водного сульфата церия (IV) до перехода оранжевой окраски раствор;! в зеленоватую.
2.12.3.3. Для определения коэффициента поправки допускается использовать растворы 5-водного серноватистокислого натрия и соли Мора 0.1 моль/дм’. при этом в формуле, как указано в н. 1.7 ГОСТ 25794.1. вместо Удолжно быть 2 К а раствор соли Мора при определении но и. 2.12.3.2 должен быть объемом 15—20 см’.
2.12.3.1—2.12.3.3. (Измененная редакция. Изм. № I).
2.12.3.4. (Исключен, Изм. № 1).
1. РАЗРАБОТАН И ВНЕСЕМ Министерством химической промышленности СССР
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета СССР по стандартам от 23.05.83 № 2303
3. Стандарт соответствует СТ СЭВ 3675—82
4. ВВЕДЕН ВПЕРВЫЕ
5. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Источник